人体的大部分组织,器官都被表皮细胞所覆盖。表皮细胞对于人体免受的刺激具有十分重要的"屏障"作用。然而,表皮细胞并不是化的,它的更新换代必须受到严格的调控才能内部组织器官的安全。尤其是当病原体通过伤口进行感染的时候,表皮细胞需要找到合适的方式尽快愈合以降低恶化程度。

I型干扰素是宿主抗病毒免疫过程中主要的效应,根据这一特性,I型干扰素及其相关很有可能对表皮细胞在应对病毒感染时的更新换代具有促进作用。然而,对这一问题的研究有很多技术难题:首先,利用真实的病毒感染模型做研究很难区分病毒与干扰素的效应;如果利用I型干扰素缺失突变体小鼠进行研究,则病毒感染又会造成很严重的症状甚至造成个体快速死亡,不利于进一步分析。
大学圣易斯分校医学院的Thaddeus S. Stappenbeck最近在《细胞:宿主与微生物》上发表了对病毒感染与表皮细胞更新换代的关系的研究。他们分别建立了两个模型:I型干扰素过表达小鼠突变体Irgm1-/-;poly(I:C)模拟病毒感染来代替之前的方法。
他们首先向野生型小鼠感染小鼠巨细胞病毒(MCMV),一周之后,发现很多原本代谢率很低的器官表皮细胞(肾脏,肝脏,胰腺,唾液腺)发生了快速的增殖与凋亡。之后,他们利用Irgm1-/-小鼠重复上述实验,得到了类似的结果。在此基础上,作者杂交获得了Irgm1-/- Ifnar-/-双突变小鼠(这种小鼠虽然过表达I性干扰素,但是缺失I型干扰素受体),并且利用双突变小鼠重复了上述实验,发现表皮细胞快速的增殖与凋亡现象并没有发生。以上实验结果说明I型干扰素的确参与了表皮细胞的快速更新。同时,作者证明了I型干扰素本身并不直接导致表皮细胞的凋亡。
为了研究I型干扰素是否参与了伤口愈合的过程,作者向Irgm1-/-小鼠,Irgm1-/- Ifnar-/-双突变小鼠以及野生型小鼠分别饲喂双氯芬酸(一类可以引起肠道溃烂的抗炎症药物),并且比较了2-4天后伤口的愈合情况。结果显示:Irgm1-/-小鼠较其它两种小鼠具有更快速愈合的能力,说明I型干扰素的确能够促进伤口的愈合。
那么I型干扰素到底是如何起作用的呢?作者首先通过杂交得到了Irgm1-/-与肠道表皮细胞性Ifnar-/-双突变小鼠(Irgm1-/- Ifnar-/-VC),并且给予poly(I:C)刺激。结果显示,此类突变体小鼠与Irgm1-/-单突变具有相似的肠道表皮更新速率,并且要明显高于其他两组小鼠。实验结果说明I型干扰素并不是直接作用于肠道表皮细胞而发挥功能的。与此相对,作者构建了Irgm1-/-与巨噬细胞性Ifnar-/-双突变小鼠(Irgm1-/- Ifnarf/f-LysM-Cre),发现这一类小鼠的肠道表皮细胞更新的速率较对照组(Irgm1-/-单突变)有了明显的下降。了巨噬细胞在响应I型干扰素进而促进表皮细胞更新过程中的作用。
接下来要问的就是在接受I型干扰素刺激后,巨噬细胞内部发生了怎样的信号传导过程。作者分析比较了Irgm1-/-单突变小鼠与野生型小鼠的个器官组水平的差异。研究发现:Apol9a与Apol9b,两个同源的干扰素诱发因子(ISG:interferon stimulatory gene),在Irgm1-/-单突变小鼠中表达量相对较高。同样,野生型小鼠在接受MCMV刺激后,各器官中Apol9a与Apol9b较未处理组也有明显的上调。
那么这两个蛋白是否就是连接巨噬细胞与表皮细胞更新的关键呢?作者设计了一段基因序列,包括细胞周期调控蛋白cdc25A及其启动子,下游连接一个荧光素酶报告基因。之后以此为模板构建了转基因小鼠。之后,作者将转基因小鼠的小肠组织取出,分别在加有Apol9A以及对照培养基中培养。一段时间之后通过荧光素酶检测分析细胞增殖的情况。结果显示:在有Apol9A存在的情况下,小肠表皮细胞增殖能力明显高于对照组。说明Apol9A能够直接促进表皮细胞的增殖。之后,作者通过蛋白水平检测,发现过表达Apol9A的肠道表皮细胞其ERK磷酸化程度明显高于对照组;另外,利用MEK 剂 U0126处理小肠组织后,apol9A对表皮细胞增殖的促进作用大幅降低了。这一结果说明了Apol9A可能是通过MEK信号通过发挥作用的。
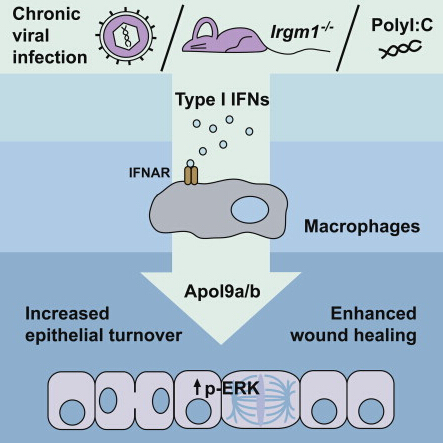
这篇研究的亮点在于发现了I型干扰素在抗病毒以外的另一功能。以往干扰素都被认为是抵抗病毒感染的利器,想不到它还具有对宿主表皮细胞的作用 。









最新评论