最新一期Cell中,报道了美国洛克菲勒大学关于丙肝病毒(Hepatitis C virus,HCV)对宿主细胞内特殊miRNA及其靶基因表达调控机制最新研究。
HCV是一种链RNA病毒,会造成肝炎、肝癌等多种恶性肝部疾病。已有研究表明,HCV感染细胞后,会利用自身基因组RNA性结合肝部表达丰富的miR-122,其自身复制也依赖于此过程。
本项研究中,研究者首先对导入了HCV的Huh-7.5肝癌细胞进行了CLIP-Seq检测,绘制出AGO在HCV RNA上的结合图谱,结果表明,AGO主要结合于HCV RNA的5UTR,E1,E2,NS5A和NS5B几个区域,这些区域正好都与miR-122种子序列重合。如果在Huh-7.5中敲除miR-122或Drosha酶,AGO在HCV RNA上的结合会明显减少,由于表达最广的前50个miRNA中没有任何一个miRNA种子序列位于AGO结合区域内,研究者认为AGO会与miR-122结合于HCV RNA上,且实验表明它们主要集中于5UTR区的S1/S2区域上。
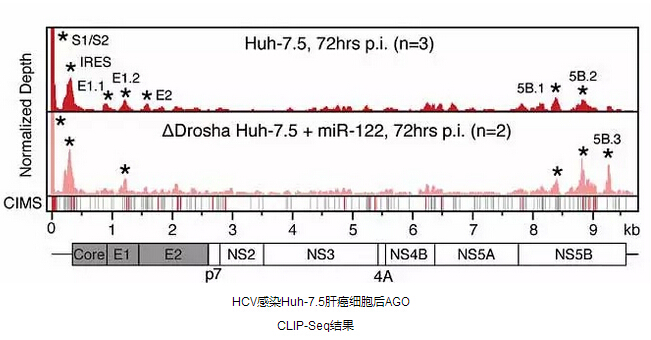
由于HCV RNA的这种miR-122“海绵”效应,研究者认为病毒可能会通过此效应减少宿主细胞内miR-122对其靶点的功能。它们比较了被HCV感染和正常细胞的RNA-Seq结果。结果表明,之前CLIP-Seq中发现的一些miR-122靶基因的确出现了上调,这些靶基因的miR-122也都存在于3UTR区域内。CLIP实验也表明,如果将Huh-7.5细胞内miR-122敲除,当HCV感染细胞时,miR-122靶基因mRNA的3UTR种子序列处AGO的结合也相应减少。这些结果直接证明了研究者关于HCV RNA感染后对宿主细胞miR-122的调控功能。
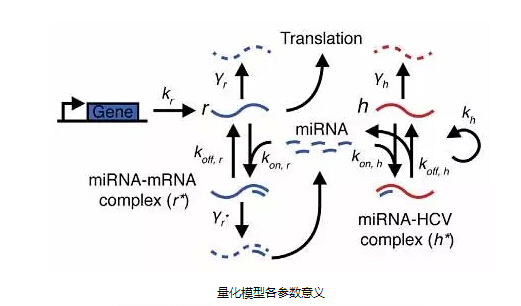
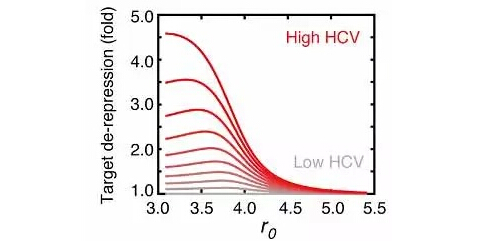
该模型中,增加HCV:miR-122结合强度或HCV丰度会造成miR-122靶点所受到的作用逐渐减弱。从上到下的曲线代表HCV以10%的梯度减少宿主miR-122储备
为了得到对HCV RNA更为量化的结论,研究者分别上调和miRNA,以控制其靶基因表达,并通过多剂量实验,得到了一个HCV RNA宿主miR-122功能受到的定量方程,分别设置了游离miRNA、miR-122结合位点数目等多个参数。通过改变这些参数,研究者可以进一步精确地拟合出HCV感染后其RNA对miR-122的吸收作用以及宿主细胞中miR-122功能缺失程度。
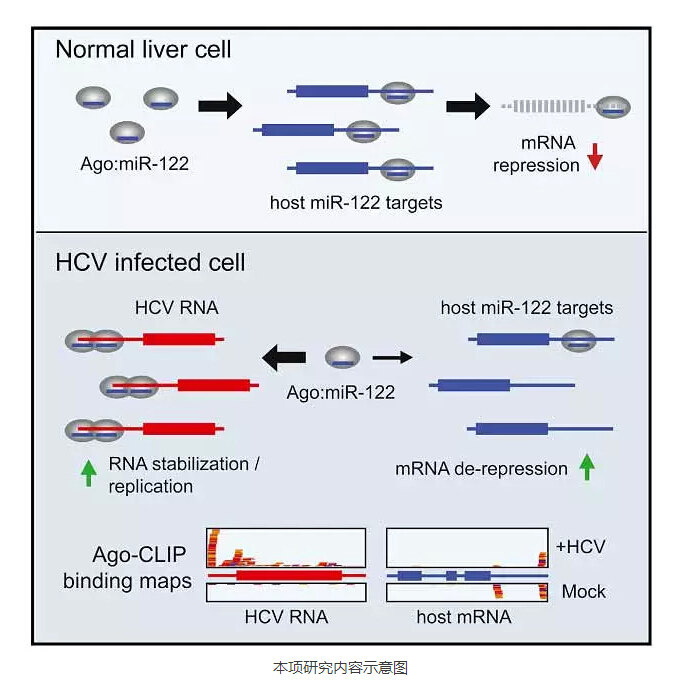
本项研究通过CLIP-Seq及RNA-Seq等多种实验手段,对HCV基因组RNA的miRNA“海绵”功能做出了更为清晰的解释,证明AGO结合于HCV RNA需要与miR-122互作才能同时结合到HCV RNA,产生一个促病毒复制的细胞,帮助病毒快速复制,造成更为严重的致病效果,为开发更为精确和可靠的肝部疾病疗法提供了更好的依据。









最新评论