癌症性单克隆抗体是抗癌疗法研发历史中最成功的药物之一。癌症性抗体不仅可以作为单独的活性药物作用于靶向癌细胞,也可以作为运输机器将药物运送到特定的位点。然而目前已知的癌症性靶点还知之甚少,许多癌症靶点还在研究中。
根据已有的信息,目前市场上一共有19种癌症抗体类药物,其中两种已经在今年1月份进入了首次常规检查程序。这19种单抗中有7种针对血液恶性肿瘤,12种用于治疗实体瘤。前者针对的靶点蛋白有四类,分别是:CD19,CD20,CD30以及CCR4,后者中有六种抗体直接针对癌细胞表面(主要是EGF-R与HER2),而剩下的单抗主要用于宿主的癌症性免疫反应,比如CTLA-4以及PD-1抗体,以及癌症的血管生成,比如VEGF抗体。总之,目前得到批准的癌症单克隆抗体覆盖面太窄,而且性也不够强。
这一不足或许是由于目前的靶点筛选方法导致的。比如通过寻找癌组织与正常组织中DNA,RNA以及蛋白质的差异寻找合适的靶点。目前我们极大地依赖于体外的癌细胞系或者临床样本进行靶点的筛选,然而体外的癌细胞系与体内中的肿瘤在很多表面的表达水平方面是存在明显差异的,而这些差异我们并不十分清楚;临床样本虽然可以提供相对真实的信息,但无奈数量太少,我们无法依靠其进行常规的筛选实验。
此外,在高通量基因组学与蛋白组学研究中,一系列前期步骤极大地了原本癌细胞的组织结构。虽然在体外检测中我们必须放弃肿瘤的复杂结构才能获得水平的信息,然而这些结构反映了肿瘤在体内的真实。肿瘤是一类复杂的组织结构,除了癌细胞本身之外,还包括多种非癌细胞,比如表皮细胞,内皮细胞,免疫细胞等。另外,还有许多可溶性地细胞因子在肿瘤的微中。除此之外,肿瘤内部还有大量的血管系统存在,它们实际上也可以作为稳定的肿瘤靶点进行研究(肿瘤内部的血管,无论其结构还是功能,都是异于正常组织的。这些血管系统可以营造局部的高血压,引起局部缺氧与再灌注,导致抗体的浸入受限)。然而这些信息在我们目前的方法中均被忽视了。
很长时间以来,研究者们均花费大量时间在肿瘤本身的研究,而忽视了肿瘤的微,最近这一现象得到了改观。很多研究开始注意肿瘤为对肿瘤生长的影响。
针对目前围绕肿瘤微设计的性抗体身份有限,作者提出了一些基于抗体展示技术的新型研究手段,或许可以帮助我们加快研发的速度。
目前已经有一些人源抗体库构建出来,体外筛选某一特定纯化抗原的抗体十分简便:只需几轮的亲和选择便可以得到。通过优化筛选条件还可以增强筛选效果。虽然抗体的天然属性无法获得,但体外筛选条件却可以得到精确调控。比如可以设计一段特定的抗原构象筛选得到性的抗原物质,又或者可以加入一段竞争性的抗原去除不想要的抗体类型。体外筛选技术可以克服体内自然形成过程中出现的免疫耐受现象,得到针对高保守的抗原或者自体抗原的抗体。
然而,抗体的实际选择过程要更为复杂一些。其中包括筛选针对整个细胞的抗体群,其中目标靶点只是细胞所有表位的一部分,而且需要对异源的细胞群进行统一筛选。这一手段效果不明显,原因性的噬菌体颗粒背景过高,选择往往偏向于高表达的表位类型以及多轮筛选后富集的往往是主导型的噬菌体克隆。在报道的筛选结果中,有一多半筛选到的抗体被证明能够与相应抗原发生性结合。这些抗原表位均为高表达的,比如EGFR,DC44,HER2等。
一些研究发现了一些新的抗原表位,他们认为需要利用新型的筛选技术找到那些低丰度的特征。其中包括正在开发的"表型筛选"技术等。
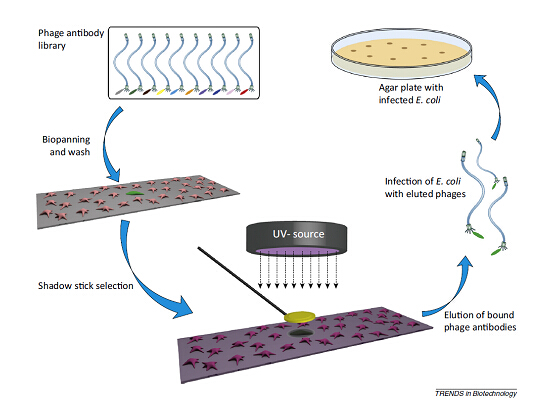
当任何组织离开其原本的生长时,都会引起明显的基因表达差异。因此,在利用细胞系鉴定得到肿瘤性标记应用到临床上时要十分小心,而且我们在筛选过程中要尽可能肿瘤组织的原生生长。另外一个问题是不同的肿瘤组织具有很强的异质性,这也对靶点的筛选造成了困难。为了解决这些问题,新型的噬菌体筛选技术被开发出来。首先需要介绍的是激光捕捉微切片(lasercapturemicrodissection,LCM),这项技术能够从与噬菌体库共培养的肿瘤组织中切出一小片细胞供后续的分析。LCM方法的关键在于切片的制备,这直接影响到最后的筛选结果。尤其是脱水步骤,这一步骤能够严重地降低噬菌体颗粒的结合。
研究者们开发出了能够兼容LCM与噬菌体活性的方法,比如在LCM之后快速冻干切片尽可能多的噬菌体颗粒的附着。
对于筛选针对肿瘤微中稀有的细胞亚群的一个关键问题是噬菌体颗粒接触受到。为了解决这个问题,S?rensen与Kristensen两人开发出了针对单个细胞的抗体筛选技术。之所以称之为"影-棍"是因为这一方法需要用到一个小圆盘粘在玻璃吸管的下方(很像曲棍球)。
这个装置用于靶细胞在辐射杀伤过程中的影响。之后就可以顺利进行噬菌体的吸附操作了。这一方法对于低丰度的细胞类型抗体筛选十分有效果。
体内的噬菌体筛选技术最大的好处在于不需要原有的肿瘤微结构。比如一类叫做avb3的整合素蛋白,它在体内性高表达与肿瘤上皮细胞,而在体外的肿瘤细胞系中这一广谱地高表达,因此如果仅靠体外筛选技术我们很容易错过这个非常好的标记。
我们通过将噬菌体库注入小鼠体内,然后分析肿瘤组织内部性附着的,同时又相对较少出现在其它正常组织中的噬菌体颗粒,就可以找到相应的性靶点。









最新评论