众所周知2017年NCCN指南更新了对于RAS野生型转移性结直肠癌的一线靶向治疗的推荐。将抗EGFR靶向治疗(西妥昔单抗和帕尼单抗)在一线治疗中的使用“仅限于原发瘤位于左侧结肠患者”。在左半结肠中无论是西妥昔单抗还是帕尼单抗,与单纯化疗或化疗联合贝伐单抗的治疗对比,均能带来显著获益;对于右半结肠癌,与单纯化疗相比,抗EGFR靶向治疗的获益则明显减少或不能获益,而应用贝伐单抗获益显著高于抗EGFR靶向治疗。本期案例为RAS野生型转移性右半结直肠癌患者,在一线标准治疗(贝伐单抗联合放化疗)后进展,应用NGS指导精准用药获益。对于这种案例及治疗方案我们该如何理解?临床上对于CAD-ALK这种罕见融合形式的肠癌病人,我们应该如何选择治疗方案?本期至本医疗科技邀请了在结直肠癌治疗方面有着丰富经验的郭元彪教授,为大家解读这一案例。该案例由国外研究者报道,发表于2015年的British Journal of Cancer上。
初诊:2012年进行标准治疗,包括右侧结肠切除术,体外照射放疗(EBRT),在放疗的前后以奥沙利铂、5-氟尿嘧啶/亚叶酸钙及贝伐单抗进行了两轮化疗。标准治疗后进展。
检查结果:2012-2015取三次活检,IHC检测原位肿瘤,淋巴结及肝转移部分都发现了ALK的高表达。
NGS检测发现了CAD-ALK的融合,结合之前的检测结果推测,ALK融合可能是关键的驱动因素。
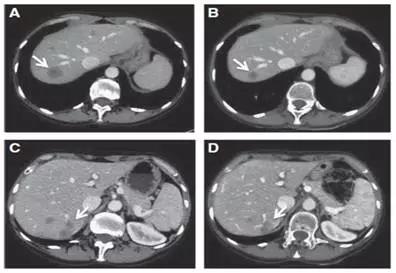
第二次治疗:病人于2015年入组entrectinib (Pan-Trk,ROS1和ALK剂)的I期临床试验 (ALKA-372-001),400mg/m2 QD。服药4周后,CT检测,结果为PR,肝部转移灶缩小38%,脑部转移部位的肿瘤稳定,无药物相关副反应发生,服药后4个月内一直都存在响应。
综述:这是一例RAS野生型的转移性右半结直肠癌患者,应用标准治疗(贝伐单抗联合放化疗)后进展,随后通过NGS检测发现CAD-ALK融合,这是一种新的ALK融合形式,并应用ALK剂entrectinib得到明显获益。这也提示我们结直肠癌的治疗中仅仅检测RAS基因的状态是不够的,同时还应关注其他基因变异,而应用NGS能帮助临床更全面的了解患者的基因变异情况,尤其是一些常规方法难以发现的罕见的基因变异及多种基因变异类型,从而指导临床的精准治疗,使更多患者受益。
“1、该患者RAS基因状态是野生型,依据NCCN指南采用标准治疗方案后很快进展,您在临床上对这类患者会如何应对?
总体来说,临床上对于患者治疗方案的制定一定是先根据指南。该患者为RAS野生型的右半结直肠癌,依据NCCN指南采用标准治疗(贝伐单抗联合放化疗)后很快进展,这时我们可能需要考虑是否同时存在某些基因的变异从而导致了患者对标准治疗方案的不。本案例中也确实看到,通过NGS发现了CAD-ALK的融合,这属于一种新的ALK融合形式,并且应用ALK剂取得了很好的临床疗效。这也提示我们在结直肠癌的治疗中只检测RAS基因可能不够的,尤其当标准治疗方案很快出现进展后。所以在这种情况下我们可以尝试对患者进行NGS检测,来获得更全面的基因变异信息,从而指导临床下一步的治疗。
“2、对于该病例CAD-ALK的融合形式,使用ALK剂取得很好的疗效,我们从中得到哪些?
本文最初通过IHC发现了肿瘤组织中存在ALK的高表达,FISH检测到了ALK的重排,进一步通过NGS检测确认和发现了这个新的CAD-ALK融合形式,并且患者对新的ALK剂响应良好。我们知道ALK基因最早是在间变性大细胞淋巴瘤(ALCL)的一个亚型中被发现的,因此定名为间变性淋巴瘤激酶(anaplasticlymphoma kinase,ALK)。随后,在发现非小细胞肺癌中有ALK基因重排之前,在弥漫性大B细胞淋巴瘤和炎症性肌纤维母细胞瘤(IMT)中分别发现了有多种类型的ALK基因重排,至此证明ALK是致癌的驱动基因。在非小细胞肺癌中最常见的ALK基因的融合是EML4-ALK,比例大约占到5%。第一个针对ALK的获批药物是辉瑞的克唑替尼,而目前临床上常用的诊断方法为FISH。但FISH的局限在于只能看到ALK是否发生重排,而不能判断出和哪个基因发生重排并且断点在什么地方。通过NGS的方法却可以实现,并指导临床用药。并且目前已经有研究发现ALK不同形式的融合对于药物的疗效也存在不同,这也告诉我们NGS可以更精准的判断基因的变异形式并指导临床更精准的用药。
“3、目前多个ALK剂已经获批上市,临床上有多个药物可以选择,而患者却直接选择入组了在研药物entrectinib的临床试验,结果病情得到很好的控制,应该怎么看这个选择?
本文中医生没有给这位患者选择已上市药物,而入组临床试验可能有以下两个原因:① 该患者存在的是CAD-ALK一种全新的ALK融合形式,目前还没有相关报道指出已经上市的几个ALK药物对此融合有效。②患者的经济条件较差,难以负担已有的ALK的靶向药物,从而入组该项临床试验。这也是临床上会经常看到的情形,对于已无标准治疗方案或不能负担的患者,积极加入相应的临床试验也不失为一个选择。
“4、随着基因检测技术的发展,临床上可能会发现更多的低频突变,罕见变异位点及变异形式等,对于这些病例的治疗应如何跟指南协调统一?
所谓的罕见其实有两种:一种就是常见瘤种的罕见基因突变,另一种是罕见肿瘤。比如本案例中在常见瘤种结直肠癌中发现的CAD-ALK的融合。针对类似的罕见或低频变异,因为患者数量少,很难做大规模的临床研究,相应的药物开发进度也相对较慢,因此循证少。所以我们看到ALK剂在ALK融合变异比例更高的非小细胞肺癌里开发的如火如荼,而在结直肠中却还没有相应的临床试验。
如何给患者用药除了指南之外还可以考虑其他不同级别的来进行参考,例如一些回顾性的分析以及很多的个案报道。我们看到非小细胞肺癌的NCCN指南里会推荐RET融合的患者使用在其他瘤种中获批的多靶点剂卡博替尼和凡德他尼。所以当应用NGS检测到一些罕见变异的情况下,其实医生会依据不同的级别来进行用药推荐,尤其在指南的标准治疗失败以后,这些基因变异指导下的“异病同治”,或许能为患者带来希望之,这也是与临床指南的一种互补。
早期结直肠癌的期相对较长,治疗方案的选择相对较多。但对于晚期结直肠癌患者,尤其是多线标准治疗失败的患者,临床手段乏善可陈。因此对于结直肠癌标准治疗失败的患者有必要尽早应用NGS检测来获得全面精准的基因变异信息,从层面明确治疗的靶点,指导临床个体化治疗。除此之外,人和肿瘤的斗争是一个哲学的问题,肿瘤细胞的基因信号通一直处于变化之中,所以才会出现某些患者刚开始治疗的疗效很好,过段时间疗效就显著下降了,甚至出现高速进展。因此NGS对肿瘤患者的动态监测来预测或药物的疗效也是一个重要的应用。
最近免疫治疗也在肠癌领域有了比较大的突破,尤其是对存在错配修复缺陷(dMMR)的患者应用PD-1抗体药物取得了比较好的疗效。而错配修复的状态也是可以通过NGS检测来确认的。所以我相信未来结直肠癌治疗的发展方向一定是精准与免疫治疗相结合。
关于本病例中提到的CAD-ALK基因融合,ALK剂等信息,我们邀请了至本医疗科技医学部的崔强进行补充解析。
ALK基因最早是在间变性大细胞淋巴瘤(ALCL)的一个亚型中被发现的,因此定名为间变性淋巴瘤激酶(anaplasticlymphoma kinase, ALK),2007年发现在肺癌患者中由于染色体倒位形成棘皮动物微管相关类蛋白4(EML4)基因与ALK 基因的融合/重排(EML4-ALK),促使肺癌发生和进展。
目前在肺癌患者中已发现至少26种具有功能活性的ALK融合变异类型,其中EML4-ALK为最常见融合类型。
ALK融合常见于不吸烟或少吸烟肺腺癌患者,阳性检出率~5%。ALK融合与EGFR突变一般是互相的。
除基因融合、基因突变外,ALK还有基因扩增和基因缺失两种变异类型,其均与ALK剂耐药相关。
当ALK激酶结构域区域发生基因突变时,其氨基酸改变影响蛋白空间结构以及ALK剂的结合,进而导致耐药现象的出现 。
该案例中,患者最初接受crizotinib治疗有效,重新组织活检发现ALK C1156Y突变,如下图所示crizotinib对C1156Y耐药,故C1156Y突变是导致该患者crizotinib耐药的主要原因。
随后,患者接受ceritinib治疗,5周后CT检查显示疾病进展并出现多个肝转移灶。如下图所示,ceritinib对C1156Y同样耐药,因此导致ceritinib治疗无效。
后续的全外显子组测序、克隆异质性分析、细胞水平试验表明,C1156Y-L1198F双重突变对crizotinib,故重新接受crizotinib治疗获益。
小结:ALK剂耐药与是否出现耐药突变位点密切相关;不同ALK剂的选择必须以精准基因检测为基础。
• FISH能和灵敏地检测出ALK融合基因,是目前检测ALK融合基因的首选方法,在克唑替尼上市时被美国食品药品管理局(Food and Drug Administration, FDA) 批准为EML4-ALK阳性NSCLC的伴随诊断方法。IHC法虽然也能够检测ALK基因融合,但其作为ALK融合基因的初筛手段,如疑似假阴性或假阳性,仍需FISH或NGS等方法确认。
•与FISH和IHC等传统方法相比,NGS一次可将所有ALK融合形式全部检测,性价比更高;NGS有助于发现新的ALK融合形式;NGS在检测ALK基因融合的同时还可检测ALK基因点突变,为后续ALK剂药物选择及耐药预测提供依据。
Entrectinib是一种多靶点酪氨酸激酶剂,分别Trk家族的三种亚型(TrkA, TrkB和TrkC),ROS-1和ALK,在体外和体内试验中均表现出活性。在AACR2016上最新的临床数据显示治疗多种NTRK融合或ROS-1融合或ALK融合的实体瘤患者,客观有效率达到了79%,并且对脑转移的患者也有效。
C.分别针对A基因5’端和B基因3’端设计一对探针将新的融合基因捕获并通过NGS测序获得一系列包含融合区域的序列(reads)。
D. 将获得的reads分别与A、B基因参考序列比对,如能够与A、B基因5’和3’端序列匹配则表明有检出融合基因。
1.转移性结直肠癌的治疗中只检测RAS基因可能是不够的,尤其当标准治疗方案很快出现进展后,有必要尽早应用NGS获得全面精准的基因变异信息,比如对于基因融合的检测,NGS可以判断出和哪个基因并以什么形式发生融合,从而指导精准用药。
2.肿瘤细胞的基因信号通一直处于变化之中,因此NGS对肿瘤患者的动态监测来预测或药物的疗效也是一个重要的应用。









最新评论